Розулип (Капсулы) в Ставрополе
Инструкция по применению Розулип
Действующее вещество
Розувастатин+ЭзетимибПоказания
Первичная гиперхолестеринемия (тип IIа по Фредриксону, включая семейную гетерозиготную гиперхолестеринемию), гомозиготная семейная гиперхолестеринемия (тип IIb по Фредриксону).
Противопоказания
Беременность и период грудного вскармливания; пациенты женского пола с детородным потенциалом, не использующие эффективные методы контрацепции; заболевания печени в активной фазе или устойчивое повышение сывороточной активности печеночных трансаминаз неясной этиологии (более чем в 3 раза по сравнению с ВГН); нарушение функции печени средней (7-9 баллов но шкале Чайлд-Пью) или тяжелой (более 9 баллов но шкале Чайлд-Пью) степени тяжести; тяжелое нарушение функции почек (КК <30 мл/мин); миопатия; одновременное применение с циклоспорином; возраст до 18 лет.
Для дозировки 40 мг + 10 мг
Наличие следующих факторов риска развития миопатии/рабдомиолиза: почечная недостаточность средней степени тяжести (КК <60 мл/мин), гипотиреоз, миотоксичность на фоне приема других ингибиторов ГМГ-КоА-редуктазы или фибратов в анамнезе, чрезмерное употребление алкоголя, состояния, которые могут приводить к повышению плазменной концентрации розувастатина, одновременный прием фибратов; пациенты монголоидной расы; анамнез наследственных мышечных заболеваний, в т.ч. семейный.
С осторожностью
Состояния, свидетельствующие о развитии миопатии или предрасполагающие к развитию почечной недостаточности, вторичной по отношению к рабдомиолизу (сепсис, артериальная гипотензия, обширное хирургическое вмешательство, травма, тяжелые метаболические, эндокринные и электролитные нарушения или неконтролируемые судороги); гипотиреоз; возраст старше 70 лет; состояния, при которых отмечено повышение концентрации розувастатина в плазме крови; пациенты монголоидной расы; одновременное применение с фибратами, антикоагулянтами непрямого действия (варфарином) или флуиндионом; миотоксичность на фоне приема других ингибиторов ГМГ-КоА-редуктазы или фибратов в анамнезе; чрезмерное употребление алкоголя; заболевания печени в анамнезе или печеночная недостаточность; почечная недостаточность легкой и средней степени тяжести (КК >30 мл/мин); почечная недостаточность легкой степени тяжести (КК >60 мл/мин) (для дозировки 40 мг + 10 мг).
Состав
| Таблетки, покрытые пленочной оболочкой | 1 табл. |
| активное вещество: | |
| розувастатин цинка | 5,34 мг |
| 10,68 мг | |
| 21,36 мг | |
| 42,72 мг | |
| (эквивалентно 5 мг; 10 мг; 20 мг и 40 мг розувастатина соответственно) | |
| вспомогательные вещества: лудипресс (лактозы моногидрат — 60,5988 (93%)/121,1976 (93%)/242,3952 (93%)/484,7904 (93%) мг, повидон — 2,2806 (3,5%)/4,5612 (3,5%)/9,1224 (3,5%)/18,2448 (3,5%) мг) — 65,16/130,32/260,64/521,28 мг; кросповидон — 2,2806 (3,5%)/4,5612 (3,5%)/9,1224 (3,5%)/18,2448 (3,5%) мг; кросповидон — 3,75/7,5/15/30 мг; магния стеарат — 0,75/1,5/3/6 мг | |
| оболочка пленочная: Opadry II белый 85F 18422 (поливиниловый спирт — 0,76 (40%)/1,52 (40%)/3 (40%)/6 (40%) мг, титана диоксид — 0,475 (25%)/0,95 (25%)/1,875 (25%)/3,75 (25%), макрогол 3350 — 0,3838 (20,2%)/0,7676 (20,2%)/1,515 (20,2%)/3,03 (20,2%) мг, тальк — 0,2812 (14,8%)/0,5624 (14,8%)/1,11 (14,8%)/2,22 (14,8%) мг) — 1,9/3,8/7,5/15 мг |
Описание лекарственной формы
Капсулы твердые желатиновые CONI-SNAP 0, без маркировки, самозакрывающиеся, с основанием желтого цвета и крышкой желтого цвета, содержащие две таблетки: таблетки розувастатина 5 мг - белые или почти белые, продолговатые, с гравировкой стилизованной буквы Е и номера 596 на одной стороне таблетки, без или почти без запаха; таблетки эзетимиба 10 мг - белые или почти белые, круглые плоские, с фаской, с гравировкой стилизованной буквы Е на одной стороне таблетки и номера 612 на другой стороне таблетки, без или почти без запаха.
Фармакокинетика
Абсорбция и распределение
Розувастатин
Максимальная концентрация розувастатина в плазме крови (Сmах) достигается приблизительно через 5 часов после приема внутрь. Абсолютная биодоступность составляет примерно 20%.
Розувастатин метаболизируется преимущественно печенью, которая является основным местом синтеза ХС и метаболизма ХС-ЛПНП. Объем распределения (Vd) розувастатина составляет примерно 134 л. Приблизительно 90% розувастатина связывается с белками плазмы крови, в основном с альбумином.
Эзетимиб
После приема внутрь эзетимиб быстро всасывается и интенсивно метаболизируется в тонком кишечнике и печени путем конъюгации в фармакологически активный фенольный глюкоронид (эзетимиб-глюкуронид). Сmах эзетимиб-глюкуронида наблюдается через 1-2 часа, эзетимиба - через 4-12 часов. Абсолютная биодоступность эзетимиба не может быть определена, поскольку данное вещество практически нерастворимо ни в одном из водных растворителей, используемых для приготовления растворов для инъекций.
Прием пищи (с низким или высоким содержанием жира) не влиял на биодоступность эзетимиба при приеме внутрь в виде таблеток по 10 мг. Эзетимиб можно применять независимо от времени приема пищи.
Эзетемиб и эзетимиб-глюкуронид связываются с белками плазмы крови на 99,7% и 88- 92% соответственно.
Одновременное применение розувастатина в дозе 10 мг и эзетимиба в дозе 10 мг сопровождалось увеличением площади под кривой "концентрация-время" (AUC) розувастатина у пациентов с гиперхолестеринемией (см. таблицу 3).
Метаболизм
Розувастатин
Подвергается ограниченному метаболизму (около 10%). Розувастатин является непрофильным субстратом для метаболизма изоферментами системы цитохрома Р450. Основным изоферментом, участвующим в метаболизме розувастатина, является изофермент CYP2C9. Изоферменты CYP2C19, CYP3A4 и CYP2D6 вовлечены в метаболизм в меньшей степени.
Основными выявленными метаболитами розувастатина являются N-десметил и лактоновые метаболиты. N-десметил примерно на 50% менее активен, чем розувастатин, лактоновые метаболиты фармакологически не активны. Более 90% фармакологической активности по ингибированию циркулирующей ГМГ-КоА редуктазы обеспечивается розувастатином, остальное - его метаболитами.
Эзетимиб
Метаболизм эзетимиба происходит главным образом в тонком кишечнике и печени путем конъюгации с глюкуронидом (реакция II фазы) с последующим выведением с желчью. Эзетимиб минимально подвергается окислительному метаболизму (реакция I фазы). Эзетимиб и эзетимиб-глюкуронид (основные производные эзетимиба, определяемые в плазме крови) составляют 10-20% и 80-90% соответственно от общее концентрации эзетимиба в плазме крови. Эзетимиб и эзетимиб-глюкуронид медленно выводятся из плазмы крови в процессе кишечно-печеночной рециркуляции.
Период полувыведения (Т1/2) для эзетимиба и эзетимиб-глюкуронида составляет примерно 22 часа.
Выведение
Розувастатин
Около 90% дозы розувастатина выводится в неизмененном виде через кишечник (включая абсорбированный и неабсорбированный розувастатин). Оставшаяся часть выводится почками. Плазменный Т1/2 составляет примерно 19 часов. Т1/2 не изменяется при увеличении дозы препарата. Средний геометрический плазменный клиренс составляет приблизительно 50 л/час (коэффициент вариации 21,7%). Как и в случае других ингибиторов ГМГ-КоА редуктазы, в процесс "печеночного" захвата розувастатина вовлечен мембранный переносчик ХС, выполняющий важную роль в печеночной элиминации розувастатина.
Линейность
Системная экспозиция розувастатина увеличивается пропорционально дозе. Фармакокинетические параметры не изменяются при ежедневном приеме.
Эзетимиб
После приема внутрь 20 мг эзетимиба, меченного 14С, в плазме крови было обнаружено 93% суммарного эзетимиба (эзетимиб + эзетимиб-глюкуронид) от общего уровня радиоактивных продуктов. В течение 10 дней примерно 78% принятых радиоактивных продуктов было выведено через кишечник с желчью, 11% - через почки. Через 48 часов радиоактивных продуктов в плазме крови обнаружено не было.
Фармакокинетика у особых групп пациентов
Возраст и пол
Препарат Розулип® Плюс противопоказан детям и подросткам до 18 лет.
Пол и возраст не оказывают клинически значимого влияния на фармакокинетику розувастатина.
Фармакокинетические показатели эзетимиба были одинаковы у детей старше 6 лет и взрослых.
Фармакокинетические данные для детей младше 6 лет отсутствуют.
У пожилых пациентов (старше 65 лет) концентрация суммарного эзетимиба в плазме крови примерно в 2 раза выше, чем у молодых (от 18 до 45 лет). Степень снижения концентрации ХС-ЛПНП и профиль безопасности были сопоставимы у пожилых и более молодых пациентов, получавших эзетимиб. Для пожилых пациентов подбор дозы препарата не требуется.
Концентрация суммарного эзетимиба в плазме крови немного выше у женщин (менее 20%), чем у мужчин. Степень снижения концентрации ХС-ЛПНП и профиль безопасности одинаковы у мужчин и женщин, принимающих эзетимиб. Поэтому для пациентов мужского или женского пола подбор дозы препарата не требуется.
Этнические группы
Фармакокинетические исследования показали приблизительно двукратное увеличение медианы площади под кривой "концентрация-время" (AUC) и Сmах розувастатина у пациентов азиатской национальности (японцев, китайцев, филиппинцев, вьетнамцев и корейцев) по сравнению с европейцами; у индийских пациентов показано увеличение медианы AUC и Сmах в 1,3 раза. Фармакокинетический анализ не выявил клинически значимых различий в фармакокинетике среди европейцев и представителей негроидной расы.
Почечная недостаточность
У пациентов с легкой и умеренно выраженной почечной недостаточностью величина плазменной концентрации розувастатина или N-десметила существенно не меняется.
У пациентов с выраженной почечной недостаточностью (клиренс креатинина (КК)
После однократного приема эзетимиба в дозе 10 мг у пациентов с тяжелыми нарушениями функции почек (n=8; КК не более 30 мл/мин/1,73 м2), значение AUC суммарного эзетимиба увеличилось примерно в 1,5 раза по сравнению со здоровыми добровольцам и (n=9). Данный результат не является клинически значимым. Для пациентов с нарушением функции почек подбор дозы препарата не требуется.
У пациента после трансплантации почки, получавшего комплексную терапию, включая циклоспорин, значение AUC суммарного эзетимиба увеличилось в 12 раз.
Печеночная недостаточность
У пациентов с различными стадиями печеночной недостаточности (с баллом 7 и ниже по шкале Чайлд-Пью) не выявлено увеличение Т1/2 розувастатина. У двух пациентов с баллами 8 и 9 по шкале Чайлд-Пью отмечено увеличение Т1/2, по крайней мере, в 2 раза. Опыт применения розувастатина у пациентов с баллом выше 9 по шкале Чайлд-Пью отсутствует.
После однократного приема эзетимиба в дозе 10 мг среднее значение AUC суммарного эзетимиба было в 1,7 раза больше у пациентов с легкой степенью печеночной недостаточности (5-6 баллов по шкале Чайлд-Пью), чем у здоровых добровольцев. В 14-дневном исследовании применения эзетимиба в дозе 10 мг в сутки с участием пациентов с умеренной степенью печеночной недостаточности (7-9 баллов по шкале Чайлд-Пью) среднее значение AUC суммарного эзетимиба увеличивалось в 4 раза на 1-й и 14-й день по сравнению со здоровыми добровольцами.
Для пациентов с легкой степенью печеночной недостаточности коррекции дозы препарата не требуется. Поскольку последствия увеличения значения AUC суммарного эзетимиба неизвестны, эзетимиб не рекомендован пациентам с умеренной и тяжелой степенью (более 9 баллов по шкале Чайлд-Пью) печеночной недостаточности.
Генетический полиморфизм
Ингибиторы ГМГ-КоА-редуктазы, в том числе розувастатин, связываются с транспортными белками ОАТР1В1 (полипетид транспорта органических анионов, участвующий в захвате статинов гепатоцитами) и BCRP (эффлюксный транспортер). У носителей генотипов SLCО1B1 (ОАТР1В1) с.521CC и ABCG2 (BCRP) с.421АА отмечалось увеличение экспозиции (AUC) к розувастатину в 1,6 и 2,4 раза, соответственно, по сравнению с носителями генотипов SLCО1B1 с.521TT и ABCG2 с.421СС.
Побочные действия
Со стороны крови и лимфатической системы: редко – тромбоцитопения.
Со стороны иммунной системы: редко – реакции гиперчувствительности, включая ангионевротический отек.
Со стороны эндокринной системы: часто – сахарный диабет.
Со стороны обмена веществ и питания: нечасто – снижение аппетита.
Со стороны психики: частота неизвестна – депрессия.
Со стороны нервной системы: часто – головная боль, головокружение; нечасто – парестезия; очень редко – полинейропатия, ухудшение памяти; частота неизвестна – периферическая нейропатия, нарушения сна (включая бессонницу и кошмарные сновидения).
Со стороны сосудов: частота неизвестна – «приливы» крови к кожным покровам, артериальная гипертензия.
Со стороны дыхательной системы, органов грудной клетки и средостения: нечасто – кашель.
Со стороны ЖКТ: часто – запор, тошнота, боль в животе, диарея, вздутие живота; нечасто – диспепсия, гастроэзофагеальная рефлюксная болезнь, тошнота, сухость во рту, гастрит; редко – панкреатит.
Со стороны печени и желчевыводящих путей: редко – повышение активности «печеночных» трансаминаз; очень редко – желтуха, гепатит; частота неизвестна – желчнокаменная болезнь, холецистит.
Со стороны кожи и подкожных тканей: нечасто – кожный зуд, кожная сыпь, крапивница; частота неизвестна – синдром Стивенса-Джонсона, мультиформная эритема.
Со стороны скелетно-мышечной и соединительной ткани: часто – миалгия; нечасто – боль в суставах, мышечные спазмы, боль в шее, боль в спине, мышечная слабость, боль в конечностях; редко – миопатия (включая миозит), рабдомиолиз; очень редко – боль в суставах; частота неизвестна – иммуноопосредованная некротизирующая миопатия, поражения сухожилий, иногда осложненные разрывом, мышечная боль, миопатия, рабдомиолиз.
Со стороны почек и мочевыводящих путей: очень редко – гематурия.
Со стороны половых органов и молочной железы: очень редко – гинекомастия.
Системные реакции: часто – астения, повышенная утомляемость.
Влияние на результаты лабораторных и инструментальных исследований: часто – повышение активности АЛТ и/или ACT; нечасто – повышение активности АЛТ и/или ACT, дозозависимое повышение концентрации КФК в плазме крови, повышение активности гамма-глутамилтрансферазы; отклонение от нормы показателей функции печени.
Взаимодействия
Противопоказанные комбинации
Одновременное применение комбинации розувастатин + эзетимиб с циклоспорином противопоказано.
Нерекомендованные комбинации
Фибраты и другие гиполипидемические препараты
Пациенты, получающие фенофибрат и эзетимиб, должны быть осведомлены о возможном риске развития желчекаменной болезни и заболеваний желчного пузыря. При подозрении на желчекаменную болезнь необходимо провести исследование желчного пузыря, и отменить прием препарата.
Одновременное применение фенофибрата или гемфиброзила с эзетимибом умеренно повышало концентрацию суммарного эзетимиба (приблизительно в 1.5 и 1.7 раз соответственно).
Гемфиброзил, фенофибрат, другие фибраты и липидснижающие дозы никотиновой кислоты (более 1 г в сутки) увеличивали риск возникновения миопатии при одновременном применении с ингибиторами ГМГ-КоА-редуктазы, возможно, в связи с тем, что данные агенты могут самостоятельно вызывать миопатию при применении в качестве монотерапии. Одновременное применение препарата в дозировке 40 мг + 10 мг с фибратами противопоказано.
Ингибиторы протеазы ВИЧ
Хотя точный механизм взаимодействия неизвестен, одновременное применение с ингибиторами протеазы ВИЧ может приводить к значительному увеличению экспозиции розувастатина. В фармакокинетическом исследовании одновременное применение 10 мг розувастатина и комбинированного препарата на основе двух ингибиторов протеазы (300 мг атазанавира/100 мг ритонавира) у здоровых добровольцев приводило к увеличению значений AUC и Сmax розувастатина приблизительно в 3 и 7 раз соответственно. Одновременное применение розувастатина и комбинаций некоторых ингибиторов протеазы ВИЧ может быть рассмотрено после тщательной оценки коррекции дозы на основании ожидаемого увеличения концентрации розувастатина в плазме крови.
Ингибиторы белка-переносчика
Розувастатин является субстратом для определенных белков-переносчиков, включая транспортер печеночного переноса ОАТР1В1 и эффлюксный транспортер BCRP. Одновременное применение розувастатина с другими лекарственными препаратами, которые являются ингибиторами этих белков-переносчиков может приводить к повышению плазменных концентраций розувастатина и повышению риска миопатии.
Фузидовая кислота
Риск развития миопатии, включая развитие рабдомиолиза может быть повышен при одновременном применении с фузидовой кислотой. При необходимости систематического применения фузидовой кислоты, розувастатин должен быть исключен из терапии.
Другие взаимодействия
Изоферменты системы цитохрома Р450
Результаты исследований in vivo и in vitro показали, что розувастатин не является ни ингибитором, ни индуктором изоферментов системы цитохрома Р450. Кроме того, розувастатин является непрофильным субстратом для этих изоферментов. Поэтому не ожидается взаимодействия розувастатина с другими лекарственными средствами на уровне метаболизма с участием изоферментов системы цитохрома Р450. Не отмечено клинически значимого взаимодействия розувастатина с флуконазолом (ингибитором изоферментов CYP2C9 и CYP3A4) и кетоконазолом (ингибитором изоферментов CYP2A6 и CYP3A4).
В доклинических исследованиях было показано, что эзетимиб не индуцирует изоферменты цитохрома Р450. Не наблюдалось каких-либо клинически значимых взаимодействий между эзетимибом и другими лекарственными препаратами на уровне метаболизма с участием изоферментов CYP1A2, CYP2D6, CYP2C8. CYP2C9 и CYP3A4 или N-ацетилтрансферазой.
Антациды
Одновременное применение антацидов снижало скорость абсорбции эзетимиба, но не оказывало какого-либо воздействия на биодоступность эзетимиба. Такое снижение скорости абсорбции не рассматривается как клинически значимое.
Одновременное применение розувастатина и суспензии антацидов, содержащей магния и алюминия гидроксид, приводит к снижению плазменной концентрации розувастатина приблизительно на 50%. Данный эффект выражен слабее, если антациды применяются через 2 ч после приема розувастатина. Клиническое значение подобного взаимодействия не изучалось.
Колестирамин
Одновременное применение колестирамина уменьшало средний показатель AUC суммарного эзетимиба (эзетимиб + эзетимиба глюкуронид) приблизительно на 55%. Эффект снижения концентрации ХС-ЛПНП при добавлении эзетимиба к колестирамину может быть уменьшен этим взаимодействием.
Антикоагулянты, антагонисты витамина К
Сопутствующее применение эзетимиба (10 мг один раз в сутки) не оказывало значимого воздействия на биодоступность варфарина и протромбиновое время в исследовании с участием 12 здоровых взрослых мужчин. Однако имеются пострегистрационные сообщения о повышении МНО у пациентов, принимавших эзетимиб одновременно с варфарином или флуиндионом. При добавлении эзетимиба к терапии варфарином (или другим кумариновым антикоагулянтом) или флуиндионом следует осуществлять мониторинг МНО.
Как и при применении других ингибиторов ГМГ-КоА редуктазы, начало лечения розувастатином или повышение его дозы у пациентов, одновременно получающих лечение антагонистами витамина К (например, варфарином или другим кумариновым антикоагулянтом), может приводить к повышению МНО. Прекращение применения розувастатина или уменьшение его дозы может приводить к снижению МНО. В таких случаях рекомендуется проводить регулярный контроль МНО.
Эритромицин
Одновременное применение розувастатина и эритромицина приводит к снижению AUC(0-t) розувастатина на 20% и Сmax розувастатина на 30%. Это взаимодействие может быть вызвано усилением перистальтики кишечника, связанного с применением эритромицина.
Пероральные контрацептивы/ЗГТ
Одновременное применение розувастатина и пероральных контрацептивов увеличивает AUC этинилэстрадиола и AUC норгестрела на 26% и 34%, соответственно. Такое увеличение плазменной концентрации должно учитываться при подборе дозы пероральных контрацептивов.
Фармакокинетические данные по одновременному применению розувастатина и 3ГТ отсутствуют, следовательно, нельзя исключить аналогичный эффект и при применении данного сочетания. Однако подобная комбинация широко применялась во время проведения клинических исследований и хорошо переносилась пациентками.
Передозировки
В литературе нет данных о передозировке розувастатина.Специфическая терапия в случае передозировки розувастатина отсутствует.
В клинических исследованиях прием эзетимиба в дозе 50 мг/сут 15 здоровыми участниками в течение до 14 дней или в дозе 40 мг/сут 18 пациентами с первичной гиперхолестеринемией в течение до 56 дней обычно переносился хорошо. У животных не отмечали токсичности после однократного перорального приема эзетимиба (5000 мг/кг у крыс и мышей и 3000 мг/кг у собак).
Сообщалось о нескольких случаях передозировки эзетимиба: они обычно не были ассоциированы с развитием неблагоприятных явлений. Сообщенные неблагоприятные явления не были серьезными.
В случае передозировки следует проводить симптоматическую и поддерживающую терапию. Следует мониторировать функцию печени и активность КФК. Польза гемодиализа маловероятна.
Фармакологическое действие
Комбинированное гиполипидемическое средство (ГМГ-КоА-редуктазы ингибитор + холестерина абсорбции ингибитор).
Розувастатин
Розувастатин является гиполипидемическим средством из группы статинов. Селективный конкурентный ингибитор ГМГ-КоА-редуктазы – фермента, превращающего ГМГ-КоА в мевалонат, предшественника холестерина.
Розувастатин увеличивает количество рецепторов ЛПНП на поверхности гепатоцитов, что приводит к усилению захвата и катаболизма ЛПНП, ингибированию синтеза ЛПОНП, уменьшая общую концентрацию ЛПНП и ЛПОНП. Снижает концентрации ХС-ЛПНП, ХС-не-ЛПВП, ХС-ЛПОНП, ОХС, ТГ, ТГ-ЛПОНП, АпоВ, снижает соотношения ХС-ЛПНП/ХС-ЛПВП, ОХС/ХС-ЛПВП, ХС-не-ЛПВП/ХС-ЛПВП, АпоВ/аполипопротеина AI (AпoAI), повышает концентрации ХС-ЛПВП и АпоАI. Терапевтический эффект появляется в течение 1 недели после начала терапии, через 2 недели достигает 90% от максимального, к 4 неделе достигает максимума и после этого остается постоянным.
Эзетимиб
Эзетимиб ингибирует всасывание холестерина в кишечнике и эффективен при приеме внутрь. Механизм действия эзетимиба отличается от механизма действия других классов гиполипидемических средств (например, ингибиторов ГМГ-КоА-редуктазы (статинов), секвестрантов желчных кислот, фибратов и растительных станолов). Молекулярной мишенью эзетимиба является транспортный белок (Niemann-Pick C1-Like 1, NPC1L1), ответственный за всасывание в кишечнике холестерина и фитостеролов.
Эзетимиб локализуется в щеточной каемке клеток тонкого кишечника и препятствует всасыванию холестерина, приводя к снижению поступления холестерина из кишечника в печень, за счет чего снижаются его запасы в печени и усиливается всасывание из крови, в то время как статины ингибируют синтез холестерина в печени. Эти различные механизмы дополняют друг друга, приводя к снижению его концентрации в плазме крови.
Источники
1. Государственный реестр лекарственных средств;
2. Анатомо-терапевтическо-химическая классификация (ATX);
3. Международная классификация болезней 10-го пересмотра;
4. Официальная инструкция производителя
Характеристики

Сертификаты Розулип

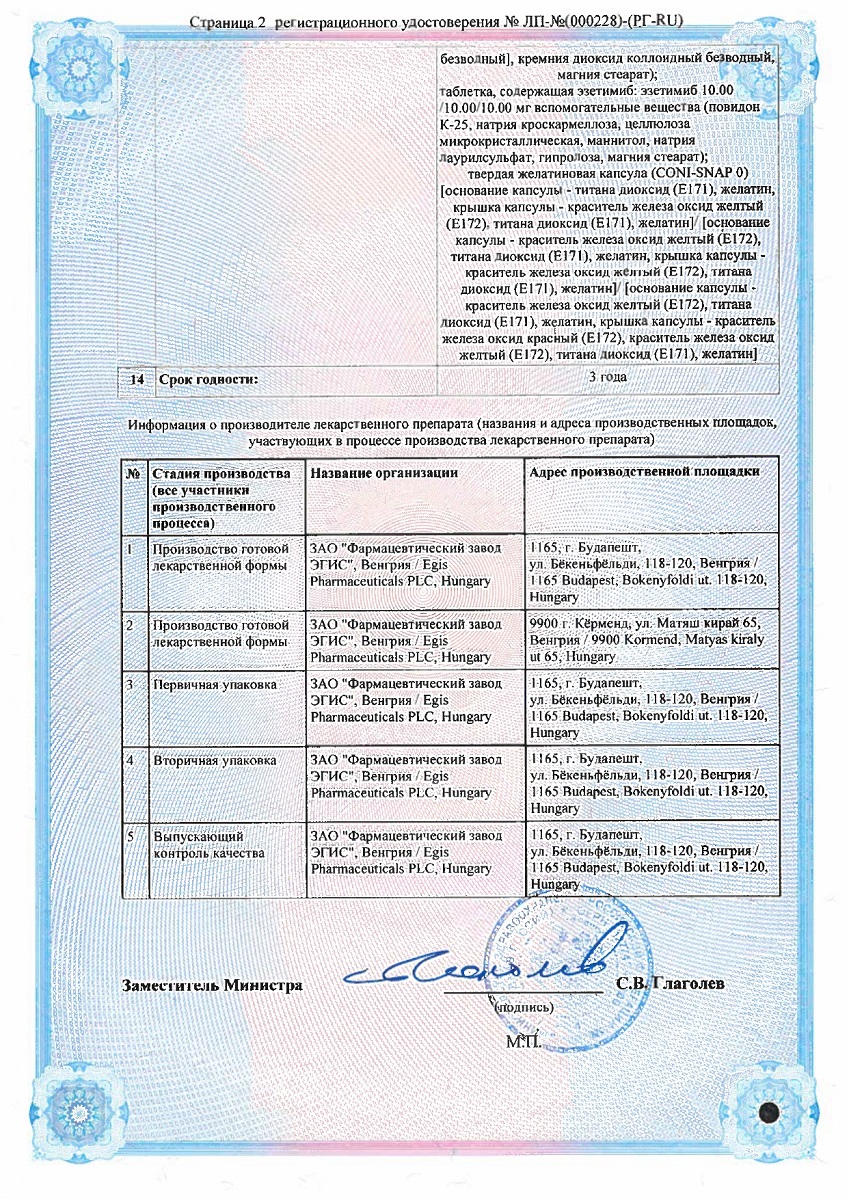



Фото Розулип